COVID-19的“候选药物”瑞德西韦尚未获批上市,但已按照“同情使用”原则在各国用于临床治疗。
4月10日,《新英格兰医学杂志》发表了一份关于在同情用药下使用瑞德西韦治疗重症COVID-19患者的研究报告。结果显示,68%的患者服药后症状改善,13%的患者完成治疗后死亡。
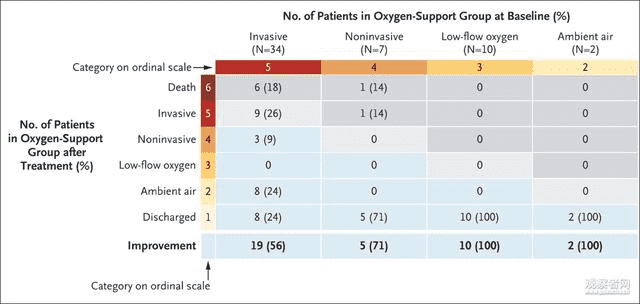
具体而言,该研究共报告了 61 名重症患者,所有患者均接受了至少 1 剂瑞德西韦治疗。其中,53人获得完整分析数据(另外8人中,7人未获得后续治疗数据,1人用药错误),分别来自美国(22例)、欧洲、加拿大(22例)和日本(9例))。治疗前,34 名患者 (64%) 需要有创通气,其中 30 名患者 (57%) 需要机械通气,4 名患者 (8%) 需要体外膜肺氧合 (ECMO) 支持。
根据治疗方案,这53名重症患者将接受瑞德西韦治疗10天,随后进行18天的随访期。
结果:53例重症患者中,36例(68%)症状缓解,30例使用呼吸机的患者中有17例拔除插管,最终出院25例; 8名患者症状恶化,其中7人(13%)死亡;其余人的症状没有变化,其中一人仍需要ECMO才能生存。
36人症状缓解
在安全性方面,共有32名患者(60%)出现了副作用,最常见的是肝酶升高、腹泻、皮疹、肾功能不全和高血压。共有 12 名(23%)患者出现严重副作用,包括多器官功能障碍综合征、感染性休克、急性肾损伤和高血压。
论文作者认为,此前在中国进行的一系列研究中,重症COVID-19患者的死亡率在17-78%之间。与这些数字相比,13%的死亡率值得注意。世界卫生组织3月1日发布的疫情报告指出,截至当时,重症COVID-19患者的死亡率高达50%。不过,4月6日发表的论文也指出,COVID-19疫情早、中、晚期的病死率可能有所不同,早期病死率相对较高。
同时,《新英格兰医学杂志》论文作者也指出了本研究的一些不足之处。由于该同情使用项目没有收集病毒载量数据,因此无法将瑞德西韦治疗的疗效与基线病毒载量和病毒抑制进行比较。之间的关系。而且,本研究中没有对照组的患者数量并不多,随访时间也相对较短。
一款原创新药从研发到上市可能需要十几年的时间。一些重症患者无法等待药物经过长期试验后获得批准。他们希望在尝试了多种失败的现有药物后,使用可能对他们有效的正在开发的新药物。正是在这样的情况下,“慈用”应运而生。 2019年8月新修订的《中华人民共和国药品管理法》第23条规定:“对正在进行临床试验、用于治疗尚无有效治疗方法的严重危及生命的疾病的药物,可以受益于医学观察,并符合规定。”与要求。根据伦理原则,经审查并知情同意后,可用于本机构开展临床试验的其他相同病情的患者。”
今年2月5日,中日友好医院王晨、曹斌团队在武汉金银潭医院进行了瑞德西韦的随机双盲试验,计划于4月27日结束。本次试验评价药物的有效性和安全性。
需要注意的是,近期,瑞德西韦的生产商吉利德也在大力宣传自己的产品。 4月4日,吉利德科学董事长兼首席执行官丹尼尔·奥戴发表公开信,表示吉利德已利用其原始库存活性药物成分大幅增加瑞德西韦的可用供应量。吉利德现有供应总量为150万剂瑞德西韦。这 150 万剂疫苗将用于临床试验、同情使用和扩大使用计划,并将在监管部门批准后捐赠用于未来的广泛使用。























还木有评论哦,快来抢沙发吧~